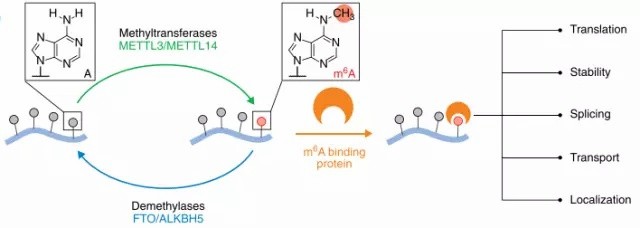
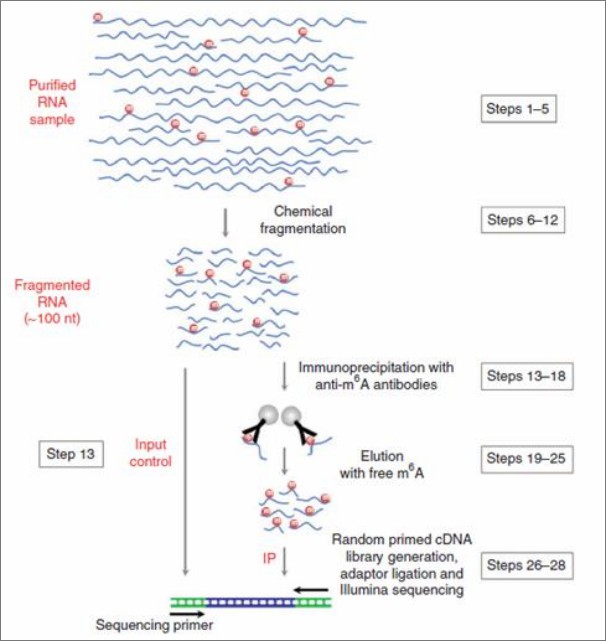
目前对m6A的转录组研究方法为MeRIP-seq(mRNA甲基化测序)的方法,其原理是通过m6A特异性抗体对细胞内具有m6A修饰的RNA片段进行免疫共沉淀,将富集下来的RNA片段进行高通量测序。结合生物信息学分析,即可在转录组范围内对m6A修饰进行系统研究。

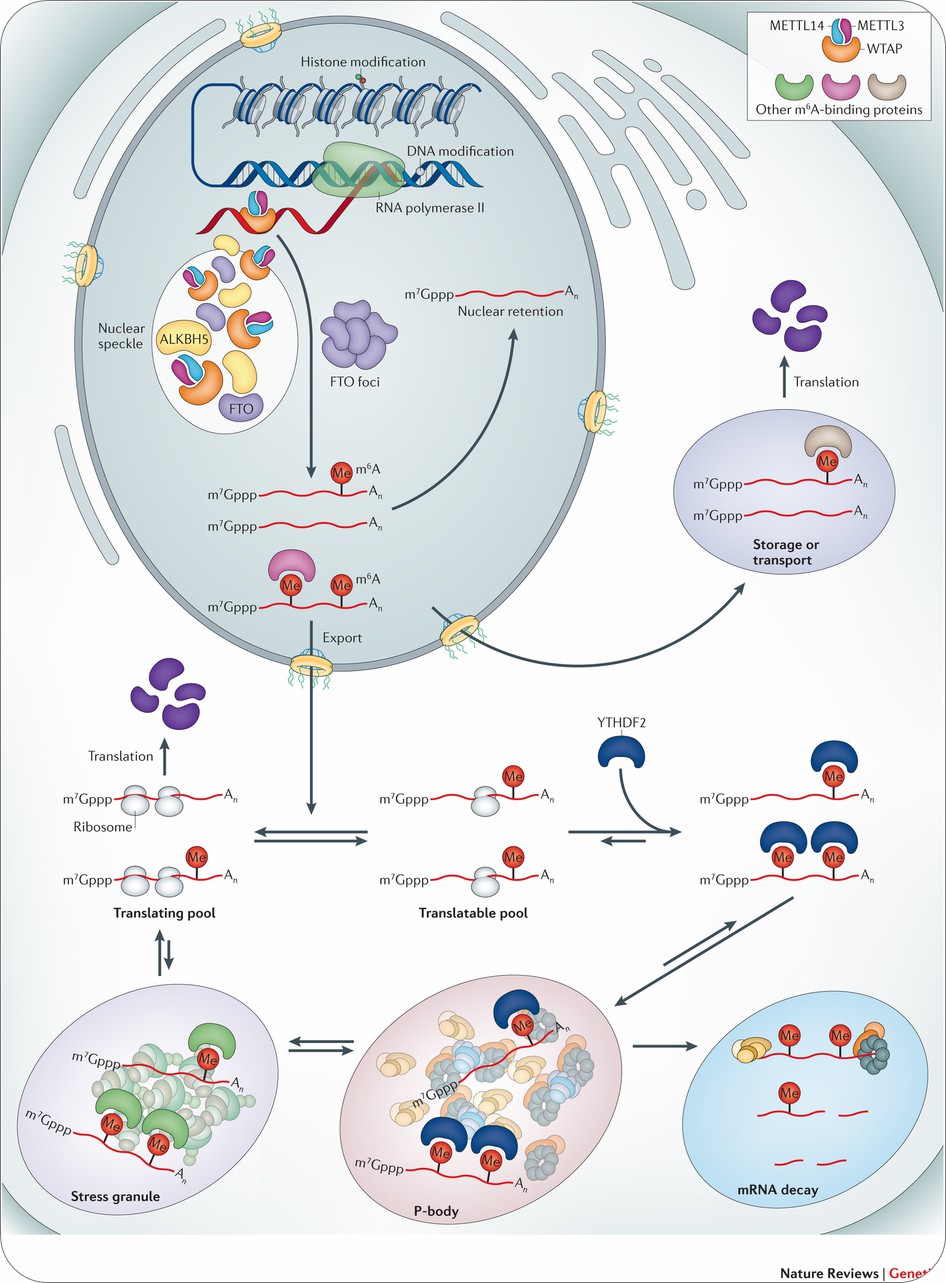
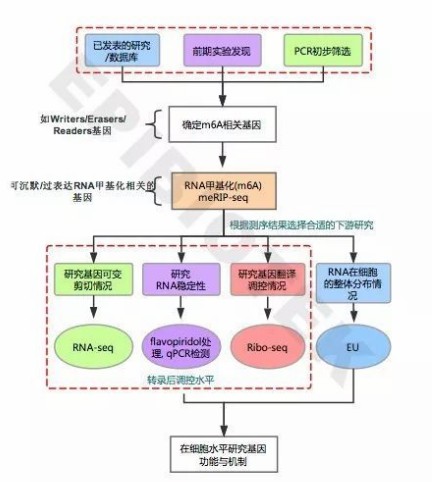
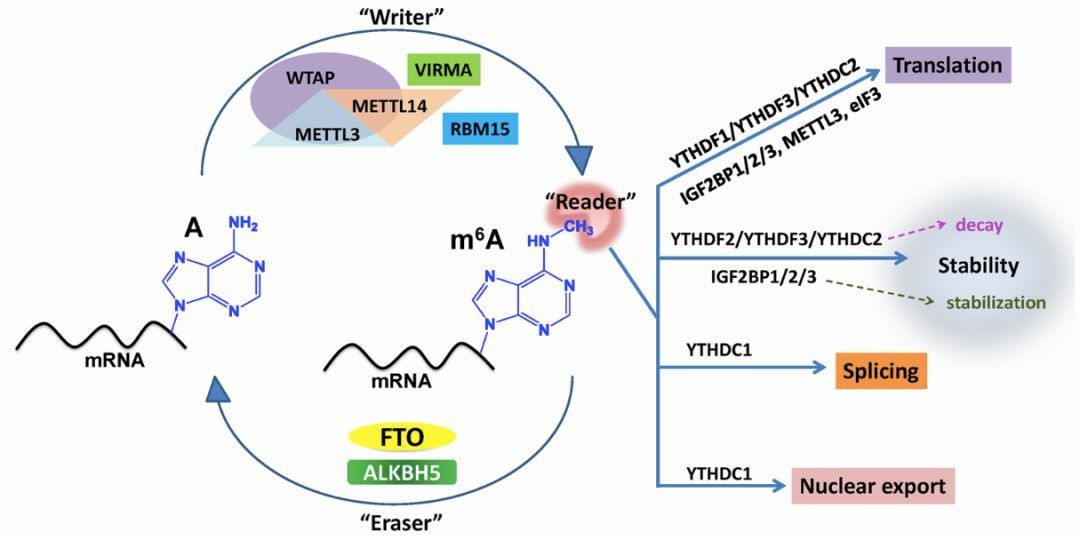
RNA 甲基化指发生在RNA 分子上不同位置的甲基化修饰现象,常见的RNA转录后修饰方式有6-甲基腺嘌呤(N6-methyladenosine,m6A) 和5-甲基胞嘧啶(C5-methylcytidine,m5C)等。
最新研究发现,m6A修饰在调控基因表达、剪接、RNA 编辑、RNA 稳定性、控制mRNA寿命和降解、介导环状RNA翻译等方面扮演重要角色。因此meRIP-seq助力解决细胞分化,生物发育、疾病发生发展,热休克反应等生物学问题。
利用甲基化RNA免疫共沉淀结合高通量测序 (Methylated RNA Immunoprecipitation sequening,MeRIP-seq)技术,可以对RNA转录后甲基化修饰图谱进行全面研究,是表观转录组学研究的关键技术。
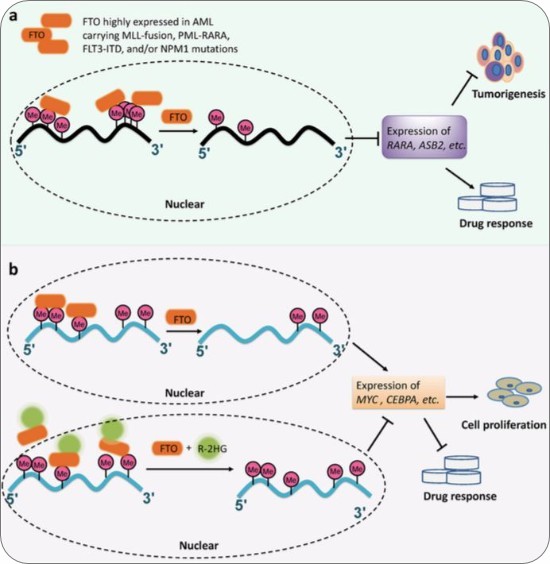
为了研究FTO对肿瘤的病理作用,研究者分析了几组急性髓细胞白血病(AML)患者大样本的全基因组基因表达数据,发现FTO在AML的某些特定亚型中高表达,包括t(11q23)/MLL-重组、t(15;17)/PML-RARA、FLT3-ITD或NPM1突变。
在体内和体外的功能获得性、缺失性实验中,他们发现FTO表达的增加,使人AML细胞存活率、增殖能力提高,促进正常造血干/祖细胞(HSPC)的癌化,并抑制ATRA诱导的AML细胞分化。重要的是,研究者发现FTO,是作为一个m6A去甲基化酶(demethylase)发挥这个作用的,它能在转录后调控它的关键靶RNA表达。
研究者还进行了全转录组m6A-seq、荧光素酶报告基因和突变实验、mRNA稳定性实验和基因特异m6A-qPCR实验,结果表明FTO通过降低m6A修饰丰度、从而降低靶mRNA转录本的稳定性,负调控ASB2和RARA表达。
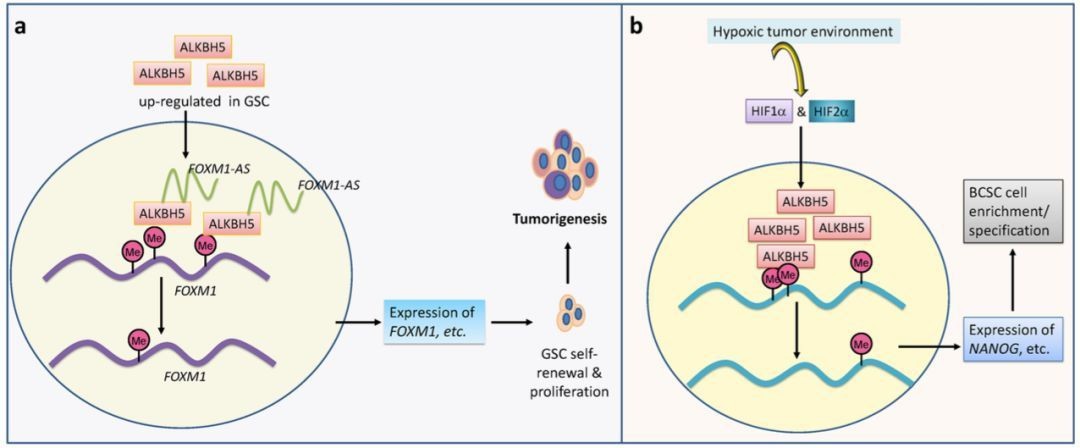
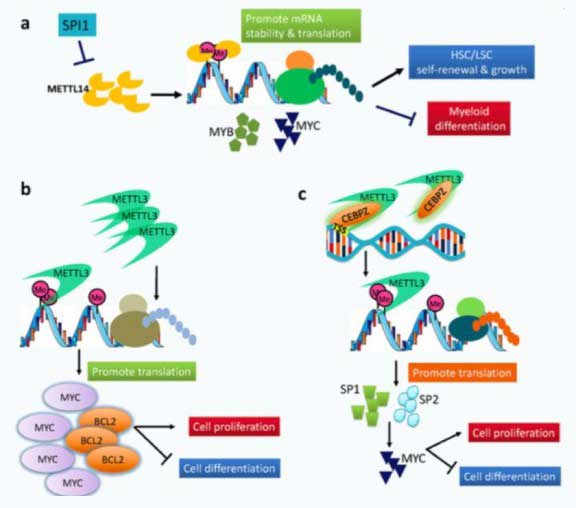


高通量测序数据日益加大,呈指数型积累上升,必须交由高速网络提速分析。
基于以色列Infiniband技术,惠研云构建优化了集群计算性能,使得计算IO提升300%,持续数据交互速率提高到2T总带宽,保证集群中任务与数据0延迟,无阻塞。